本文将继续为大家介绍《利用负载型镍催化剂的氢载体生产和利用》,点击链接☞ 《氢载体生产和利用(1)》即可回顾前文内容。
3、氨制氢
3.1 氨分解
氨具有比甲基环己烷更高的氢重量比,其沸点较高,所以在温和的条件下可以液化(大气压下-33.3℃或20℃下8.46atm)。氨是最基本的工业化学品之一,因此其处理和运输系统在世界范围内都很完善。氢可以通过如下的吸热过程制取:
.png)
在大气压和400℃的条件下,氨的转化率在热力学上可以达到约99%。催化氨分解包括氨的吸附、被吸附氨的逐步氢解离以及氮和氢原子的复合解吸14)。到目前为止,已经对该反应机理进行了广泛的研究15)~21)。在反应中,广泛认为氮解吸具有重要的动力学意义。氨的氢解离被认为是一个缓慢的过程。另外,氢会抑制该反应,特别是在低温或低氨分压下。
此前研究人员已经对氨分解催化剂进行了大量研究。Ru金属的氮键能适中,因此Ru催化剂对氨分子的吸附和氮原子的解吸均表现出较高的活性22)。此外,改变Ru金属的电子状态是提高活性的关键。然而,考虑到贵金属储量有限、成本高,开发一种由贱金属组成的催化剂是可取的。
因此,研究人员对负载在各种金属氧化物上的氨分解用镍催化剂进行了研究。先前的研究发现,尽管氧化镧的表面积较低,但其是有效的载体材料。此外,在Ni催化剂中加入的La和Ce成分提高了其活性24),25)。因此,研究人员认为,稀土成分可以提高Ni催化剂的活性。采用不同的稀土氧化物作为载体或添加剂制备了Ni催化剂,并以此分析了Ni颗粒的分散性、氨分解活性以及反应过程中反应物和产物的行为26),27)。
3.2 稀土氧化物负载型镍催化剂的研究进展
研究人员选择Al2O3、Y2O3、ZrO2、La2 O3、CeO2和Sm2O3这几种稀土氧化物作为Ni催化剂的载体材料,用于氨分解。通过浸渍法制备催化剂,并在600℃下煅烧5h26)。
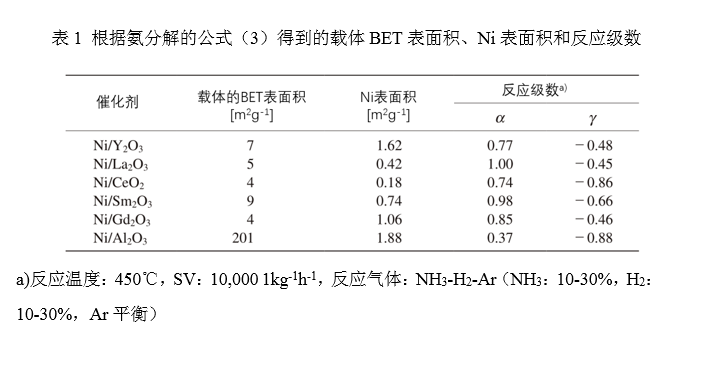
采用N2吸附BET法测定了载体的比表面积。假设催化剂表面的每个Ni原子上都有CO的单分子吸附,用CO脉冲法估算了在600℃下催化剂的Ni表面积。结果如表1所示。稀土氧化物的比表面积远小于Al2O3。一般来说,高表面积的载体材料是分散金属催化剂的理想材料。不过,一些稀土氧化物负载型催化剂表现出较高的Ni表面积。特别是Ni/Y2O3催化剂的比表面积值与Ni/Al2O3催化剂相当,表明Y2O3载体对Ni颗粒的分散是有效的。
为了解载体材料上的高Ni分散,研究人员研究了Y2O3载体在制备过程中的结构变化。催化剂制备时硝酸镍溶液的pH值低于2,因此用pH<2的硝酸溶液处理Y2O3载体,将所得粉末在600℃下煅烧。用X射线衍射(XRD)检测了Y2O3载体的晶体结构(图6)。
根据图6中2θ=29°处的峰值估计了Y2O3的晶粒尺寸。酸处理后,Y2O3相的衍射峰明显减弱,Y(NO3)3·H2O相清晰显现,说明Y2O3载体与硝酸发生了部分反应。煅烧后,Y2O3相恢复。酸处理使Y2O3相的晶粒尺寸由48nm减小到19nm,由此导致Y2O3的比表面积扩展到50m2 g-1。因此,Ni/Y2O3催化剂的高Ni分散是由Y2O3载体在浸渍过程中的微观结构变化所致。
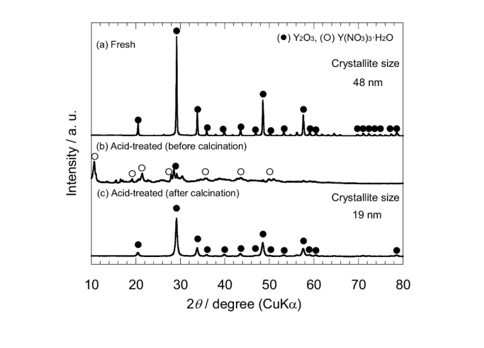
图6. (a)和(b)分别为未处理的Y2O3和酸处理的Y2O3在煅烧前的XDR图谱,(c)为酸处理的Y2O3在煅烧后的XDR图谱
对氨分解催化剂的活性进行了评价。在测试前,催化剂样品在600℃下还原2h。图7示出氨在催化剂上的转化率。所有催化剂的氨转化率从350℃开始升高。Ni/Y2O3、Ni/Sm2O3和Ni/Gd2O3催化剂的性能优于Ni/Al2O3。Ni/Al2O3催化剂的Ni比表面积最高,稀土氧化物载体对Ni催化剂的活性有积极的影响。在550℃时,Ni/Y2O3的氨转化率达到87%。与其他稀土氧化物负载催化剂相比,高Ni比表面积可能是其高性能的原因之一。一些研究人员指出Ni颗粒大小对氨分解活性的重要性28),29)。Li等人认为,随着将Ni颗粒尺寸减小至3nm,催化剂的活性增强28)。因此,在本研究中,Y2O3载体上的小颗粒有助于
