本文3920字,阅读约需10分钟
摘 要:将不含硫化物基固体电解质的碳包覆SiO(SiO-C)涂覆在集电器上,制成的片状电极,可作为全固态电池的负极。对于使用硫化物基固体电解质的全固态电池,SiO-C片状电极在室温下表现出高容量(约1500 mAh g-1),良好的循环和高速率放电性能。值得注意的是,SiO-C薄膜电极与全固态电池硫化物基固体电解质之间形成新型离子—电子传导界面。
关键字:锂离子电池、全固态电池、固体电解质、SiO-C涂层电极
近年来,采用离子传导性无机固体电解质的全固态电池在提高安全性和可靠性,扩大使用温度范围等方面备受期待。这种全固态电池有望应用于大型蓄电设备和电动汽车等。特别是Li2S-P2S5系硫化物固体电解质粉末,具有良好的成形性,通过加压压制,可以在室温下形成10-4~10-2 S cm-1级别的高锂离子传导性固体电解质层1-3。一般来说,全固态电池由这样的固体电解质层、正极层和负极层三层构成,正极层和负极层中同样含有固体电解质材料作为离子传导路径。将已经应用于使用有机电解液的锂离子二次电池(LIB)中的石墨粉末与固体电解质粉末混合,作为全固态电池的负极材料,尝试作为全固态电池的负极层4-8。然而,由于需要使正极层和负极层中含有固体电解质层以形成离子路径,导致能量密度降低。
近年来,为实现LIB的高能量密度,具有高理论容量9和低工作电位10的硅负极材料受到关注。但是,在使用有机电解液的LIB中,硅负极材料在充放电反应时的巨大体积变化(> 300%)会导致粒子粉碎和电极结构崩坏,引起导电路径的断裂和过剩的电解液还原分解,由此产生的结果就是容量急剧下降。
另一方面,目前正在研究体积变化比硅小(约200%)的SiO负极。以下(1)~(3)式示出了SiO材料的电极反应³:式(1)对应第一个循环的充电反应,式(2)对应第一个循环的放电反应,式(3)对应第二个循环以后的充放电反应。第一循环中充电时形成的Li4SiO4有望表现出锂离子传导性。
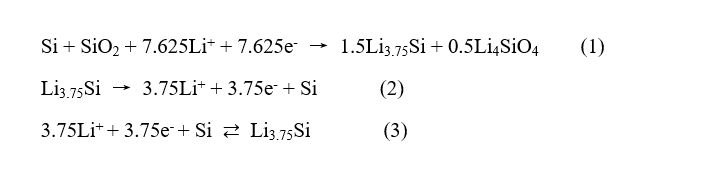
此外,还探讨了在SiO粒子表面包覆一层可起到导电助剂作用的碳,从而形成SiO-C复合物材料11,14。SiO-C复合物通过Si与SiO2以50:50的比例形成岛状晶体结构从而减少膨胀。而且,即使发生体积变化,由于导电碳的包覆,也能防止SiO粒子之间和集电体的导电路径断裂。因此,与硅负极相比,有望抑制充电循环带来的容量下降。
本研究中,将仅采用SiO-C复合物和粘结剂而不含固体电解质的涂层电极,与硫化物系固体电解质直接结合,制成全固态电池。结果显示,SiO-C涂层电极可在室温下充放电,单位重量具有约1500mAh g-1的高容量。此外还表现出稳定的容量变化,在较高的电流密度(1.0mAcm-2)下也能放电。
2.1 涂层电极的制作和全固态半电池的构建
首先,介绍SiO-C涂层电极的制作方法。采用SiO-C(碳涂覆量:5wt%;碳涂覆厚度:40~50nm,平均粒径:5µm;通过X射线衍射测定计算出Si的微晶尺寸:约4.4nm)粉末,与聚酰胺酸溶液和1-甲基-2-吡咯烷酮(NMP)溶液(纯度:99.5%,岸田化学)在空气中制成浆料。接下来,将得到的浆料涂覆在铜集电体(厚度约10µm)上,在80℃下干燥2小时。之后,在250℃下进行48小时的减压干燥,使前驱体聚酰胺酸溶液发生聚酰亚胺化,作为粘结剂。随后,将涂层电极片制成直径10mm的圆片。将成型的电极在120℃下进行10小时的减压干燥,制成SiO-C涂层电极(负极活性物质重量:1.9~2.1mg cm-2)。对得到涂层电极进行调整,使SiO-C粉末和粘结剂之比为85:15(wt%)。
用于评价的全固态半电池(half cell)采用SiO-C涂层电极作为评价电极,另一极为Li-In合金,使用硫化物系非晶质无机固体电解质(a-Li3PS4)作为电解质,在氩气氛的手套箱中用单轴冲床(300 MPa)制作而成。图1为评价用全固态半电池的示意图。使用的非晶质固体电解质(a-Li3PS4,平均粒径:5µm,室温导电率σ25 =3~4×10-4Scm-1),利用行星球墨机(FritschP-7)将硫化锂(Li2S,纯度:99%,高纯度化学社)和五硫化二磷(P2S5,纯度:99%,Aldrich)以75:25(mol%)的比例混合制成15。
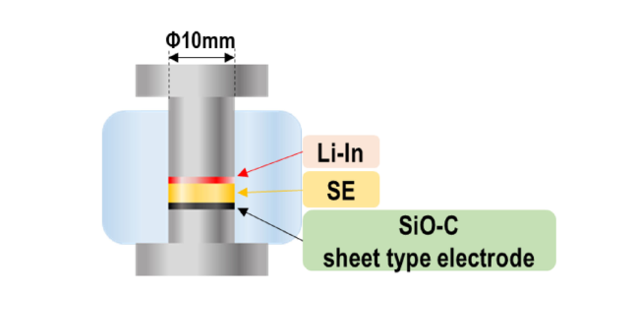
图1. 全固态半电池的示意图
2.2 全固态电池的性能评价
充放电试验采用电池充放电测试装置(北斗电工,HJ1001SD8),在电流密度为0.064mAcm-2(0.01~0.02 C-rate),恒压充电的截止电流为5µA,室温,电压范围为-0.6~0.9V vs. Li-In的条件下反复进行恒流-恒压充电与恒流放电。用电压变化量对充放电试验中获得的充放电容量进行微分得到dQ/dV图。
另外,放电速率试验是在进行上述的充放电试验后,将放电电流密度从0.064 mAcm-2变化到1.0 mAcm-2(约为初次放电电流密度的16倍),进行定电流放电。与进行上述充放电试验的全固态半电池的充电状态相反,交流阻抗测定采用电化学测定装置(Biologic,VSP-300),在室温,外加电压10 mV,频率范围为10 mHz~5 MHz的条件下进行。利用扫描电子显微镜SEM(JEOL,JSM-6510)观察充放电前后固体电解质与SiO-C电极界面的接合状态。
3.1 固体电解质-SiO-C电极界面的SEM观察
图2的SEM图像为本研究制作的全固态半电池中固体电解质与SiO-C电极接合部的截面图。从该SEM图像中可以确认,通过单轴冲压制成的评价用全固态半电池中固体电解质与SiO-C电极之间形成了良好的界面。因此,固体电解质和SiO-C电极之间可以实现锂离子的移动。

图2. SiO-C电极和a-Li3PS4固体电解质层截面的SEM图像。
3.2 充放电特性
图3所示为在电流密度为0.064mAcm-2,温度为室温下的第1次循环和第15次循环的充放电曲线。另外,图4中示出了与图3的充放电测定结果相对应的dQ/dV图。由图可知,全固态电池中的SiO-C电极可在室温下充放电,第1次循环的充电容量约为2400mAhg-1,放电容量约为1500mAhg-1。在第1次循环的dQ/dV图中,充电时的电位范围0.2~0.7 V vs. Li/Li+的还原峰值(A)是由于Li4SiO4的形成导致的,其是造成Li-Si合金化和初期不可逆容量的主要原因16。
另外,第1次循环放电时的电位范围0.2~0.6 V vs. Li/Li+的2个氧化峰值(B)是由Li-Si合金的锂离子脱离反应引起的17。此外,第15次充电时的还原峰值变为2个较宽的峰值,这与在使用有机电解液的LIB中,锂离子插入Si负极的2个非晶质层时的峰值模式类似17。这样的结果表明SiO-C电极与锂离子传导性有机电解液中的电极反应类似。