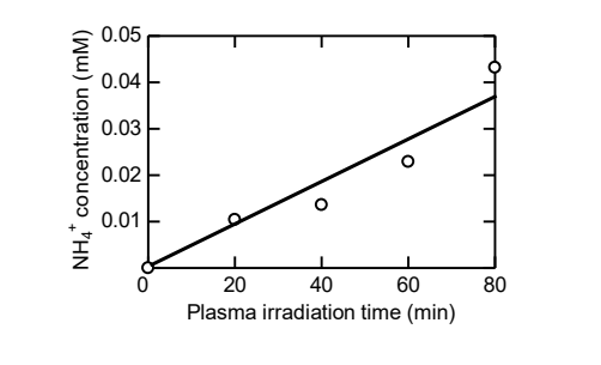
摘 要:氨(NH3)是一种极其重要的化肥原料。NH3可通过在空气中用常压氩(Ar)等离子体射流辐照水而制得。在不同的等离子体辐照时间、施加电压和等离子体辐照距离下,测量水中铵离子(NH4+)的浓度。生成的NH4+浓度几乎与等离子体辐照时间和施加电压成正比。本研究中获得的最大NH4+浓度为43.2µM,施加电压为10kV,氩气流速为10L/min,等离子体辐照距离为10mm,等离子体辐照时间为80min。在等离子体辐照期间,水温约为26℃。
关键字:常压等离子体、氨合成、室温、NH4+浓度、常压Ar、蒸馏水
1、引言
顾名思义,常压等离子体就是在常压下产生的等离子体。与低压等离子体相比,常压等离子体具有电子的温度高于离子的温度、电子能量高的特征。1、2目前常压等离子体常用于进行固体材料的表面处理、3-5水的净化、6、7细菌和霉菌灭活8、9等的研究。特别是近年来,在医学领域的应用研究较多,伤口治疗、10、11癌症治疗、12、13细胞内的遗传因子导入和药物分子导入14-16等的研究十分活跃。
氨(NH3)被用于肥料、炸药、塑料、合成纤维和树脂以及各种其他化学品的合成。17-19根据美国地质调查所(United States Geological Survey; USGS)的调查报告,1995年世界氨产量约0.96亿吨,202019年约1.50亿吨,2124年间增加了约1.6倍,其中约80%用于化肥生产。22、23氨已成为生产人类赖以生存的食物必不可少的化学合成品。而且,最近氨有望用作实现氢能社会所必需的燃料电池中的氢能载体,以及易于液化且易于处理的能源。24
目前氨的工业合成一般采用哈伯-博施(Haber-Bosch)法。1909年,Haber以锇(Os)为催化剂,在500~600℃、200气压下,使氮气(N2)与氢气(H2)反应,成功合成氨。25德国BASF公司的Bosch等人推动了其工业化,1912年BASF公司的Mittasch等人使用混合2~6%氧化铝(Al2O3)和0.2~0.6%氧化钾(K2O)的四氧化三铁(Fe3O4)催化剂来代替Os催化剂,降低了温度(450℃)和压力(100atm)。26、27
由于哈伯-博施(Haber-Bosch)法的工艺过程需要高温高压且消耗大量能源,因此开始研究合成方法的降温减压。1971年,Ozaki等人使用钌(Ru)-碳(C)-钾(K)催化剂代替铁类催化剂,实现了低温(146℃)和低压(600mmHg)。281972年,Aika等人发现,将Ru-C-K催化剂中的K替换为铯(Cs),则催化活性会进一步提高。292003年,Yandulov和Schrock的研究提出,如果使用具有三酰胺单胺四齿配体的钼(Mo)氮络合物,则可以在室温和1个大气压下合成氨。30自此,许多研究都报告了使用各种催化剂成功在室温和1个大气压下合成氨。2011年,Arashiba等人使用具有PNP型钳形配体的氮分子交联双核Mo络合物,31Yahya等人使用Mn0.8Zn0.2Fe2O4纳米颗粒,在1T磁场中实现氨合成。322012年,Kitano等人使用一种带有固定化Ru纳米粒子的电子催化剂,332017年,Chen等人使用基于碳纳米管的电催化剂实现氨合成。342018年,Kitano等人使用了一种将Ru纳米粒子固定在添加有钡(Ba)的氨基钙(Ca(NH3)2)上的催化剂。35
上述使用催化剂的方法以Ru、Mo、Ba等稀有金属为催化剂,成本高,制作过程繁琐且耗时。因此,正在研究不使用催化剂的方法。1998年,Marnellos和Stoukides通过在N2气体和H2气体中的钯(Pd)电极中通入2mA/cm2以下的电流,在570℃和1个大气压下实现了氨合成。36
此外,由于使用H2气体,因此需要制造氢气。氢气一般通过天然气、石油、煤炭等化石燃料制得。在氨合成工厂,制氢工艺占其设备的大部分,氨合成过程总能耗的90%以上用于制氢。包括制氢在内,目前常用的哈伯-博施氨合成法耗费大量能源。37因此,如果可以不使用H2气进行氨合成,则可以降低能耗。
2016年,Haruyama等人研究出在室温和1个大气压下不使用催化剂和H2气体的氨合成法。38他们通过将紫外线(UV)照射与空气等离子体或N2等离子体相结合,成功地使用水代替氢气,在水中生成氨。
本研究此前使用常压氩(Ar)等离子体射流,进行有色废水的脱色研究。39-41在这些研究中发现,当用常压Ar等离子体射流辐照蒸馏水时,蒸馏水中会生成过氧化氢(H2O2)42、43以及硝酸(HNO3)和亚硝酸(HNO2)44、45。在这些研究中,讨论了空气中N2分子解离产生N自由基的可能性,以生成HNO3和HNO2。NO3和NO2由N自由基氧化反应生成。氧化反应所需的氧(O)自由基被认为是由空气中的氧(O2)分子解离而生成的。该N自由基和O自由基结合生成NO3和NO2。正是等离子体中的高能电子导致N2分子和O2分子解离。当这些高能电子与水(H2O)分子碰撞时,H2O分子解离为氢(H)自由基和羟基(OH)自由基。OH自由基相互键合生成H2O2。结果表明,N自由基和H自由基的结合可以生成氨(NH3)。
本文中,将对常压Ar等离子体射流辐照蒸馏水生成氨,以及铵离子(NH4+)浓度与等离子体辐照时间、施加电压、等离子体辐照距离的关系进行介绍。此外,将使用热像仪观察等离子体辐照时蒸馏水的温度变化,以阐明温度变化。
2、方法与材料
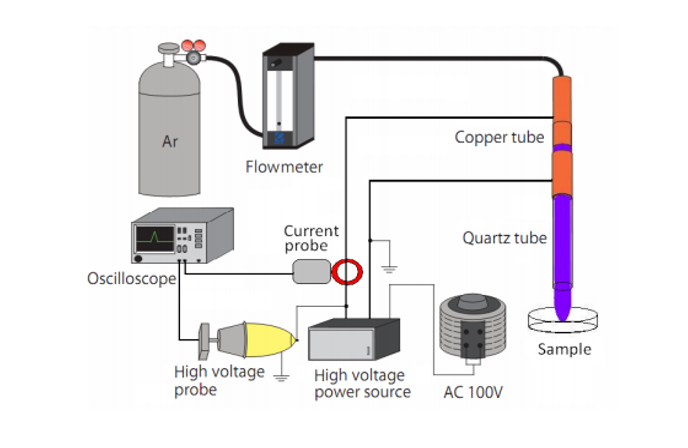
图1.实验装置示意图
图1为实验装置示意图。等离子体射流发生部分的结构为,在介质石英管(长度50mm、内径6mm、外径8mm)中插入作为放电电极的铜管(内径4mm、外径6mm),在石英管的外侧缠绕作为接地电极的铜箔(厚度0.05mm、宽度10mm)。通过施加交流高电压,在电极间的石英管内部产生介质阻挡放电,使流入的Ar气体等离子体化,等离子体向大气中喷射形成射流。等离子体射流使用Logy高压电源LHV-10AC,频率固定为10kHz,Ar气体流量固定为10L/分钟,施加电压8~10kV,辐照距离(从石英管前端到液面)2~40mm,在直径60mm的玻璃培养皿中放入20mL蒸馏水辐照0~80分钟。气体流量的测定使用Kofloc气体流量计RK-1250。使用Tektronix数字示波器TDS1001B、高电压探头P6015A和电流探头A621,测量电压和电流值。使用SANWA SUPPLY瓦特监视器TAP-TST8N测量等离子体辐照过程中的耗电量。等离子体辐照期间的耗电量约为20W。
采用毛细管电泳系统(Agilent,G1602A)测定蒸馏水中的NH4+浓度。以10mM咪唑、5mM乳酸和0.5mM 18-crown-6的混合溶液作为电泳溶液,并用1M乙酸将pH调节至4.5。以内径50µ的熔融石英管作为毛细管。通过间接吸光光度法进行检测,施加电压30kV、检测波长310nm(带宽20nm)、对照波长215nm(带宽10nm)。
使用NEC Avio热像仪F30测定等离子体辐照过程中的蒸馏水温度。
3、结果与讨论

图2.喷射到蒸馏水上的等离子体射流图片
(施加电压10kV;辐照距离15mm)
图2为等离子体辐照蒸馏水的图片。在等离子体中出现了许多看起来像白线的流光,它们击中了蒸馏水。因此认为,等离子体中的高能电子也到达了蒸馏水表面。